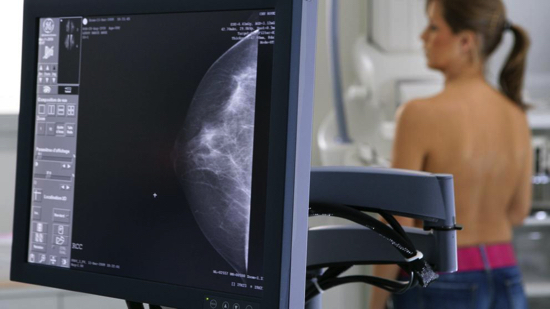
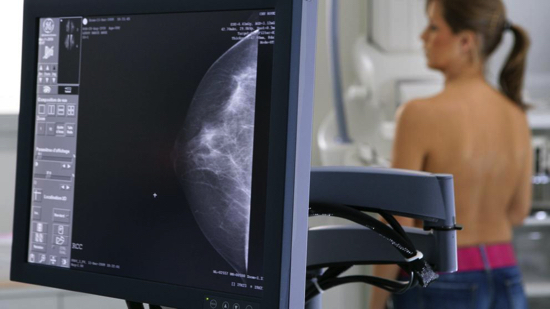
Investigadors de l’hospital Memorial Sloan Kettering de Nova York han descobert per què el càncer de mama metastàtic es torna resistent als fàrmacs desenvolupats contra la seva alteració genètica més comuna. L’ avenç, presentat en l’últim número de la revista Science, obre una via de tractament contra aquest tipus de càncer que sol tenir mal pronòstic.
“Ja estem treballant per desenvolupar nous tractaments a partir d’aquests resultats”, destaca Josep Baselga, director mèdic de l’hospital Memorial Sloan Kettering, que ha liderat la investigació.
A més de la seva transcendència clínica, la investigació és important també des d’un punt de vista conceptual perquè estableix per primera vegada la influència d’alteracions epigenètiques en l’evolució del càncer de mama. A diferència de les mutacions genètiques, que modifiquen de manera irreversible l’ADN de les cèl·lules, les alteracions epigenètiques modifiquen el nivell d’activitat dels gens i en teoria són reversibles.
La investigació s’ha centrat en el grup majoritari de càncer de mama, anomenat de receptors d’estrògens positius, que representa el 70% de tots els casos de la malaltia. Dins d’aquest grup, la mutació més comuna afecta el gen que produeix la proteïna PI3K, que es dona en el 43% de les pacients amb receptors d’estrògens positius. Aquesta proteïna coordina funcions essencials de les cèl·lules com el creixement i la supervivència. Quan està alterada per la mutació genètica, afavoreix la progressió del càncer.
Per això el desenvolupament de fàrmacs inhibidors de PI3K, que encara no estan comercialitzats, ha estat rebut com un prometedor avenç en el tractament dels càncers de mama metastàtics. Els primers estudis amb aquests fàrmacs van confirmar que tenen una potent acció antitumoral. Tot i això, els assajos clínics presentats els dos últims anys han revelat que l’eficàcia d’aquests fàrmacs dura poc, perquè el càncer aviat s’hi torna resistent. Aquesta adaptació tan ràpida de les cèl·lules tumorals ha sorprès els investigadors, que esperaven beneficis més duradors dels inhibidors de PI3K. Ara Baselga i el seu equip han trobat l’explicació.
Els assajos clínics han mostrat que quan s’inhibeix la proteïna PI3K s’acaben reactivant els receptors d’estrògens, cosa que indueix la proliferació de les cèl·lules tumorals. A partir d’aquesta observació, els investigadors han analitzat l’epigenoma de cèl·lules de càncer de mama obtingudes de pacients tractades amb inhibidors de PI3K.
L’anàlisi revela que aquests fàrmacs desencadenen un efecte dòmino a l’interior de les cèl·lules que acaba estimulant els receptors d’estrògens. La peça clau en aquest efecte dòmino és una proteïna anomenada KMT2D, que s’activa amb els receptors de PI3K i desencadena una cascada de reaccions bioquímiques.
En experiments realitzats amb cèl·lules de biòpsies de pacients s’ha confirmat que, quan s’elimina la proteïna KMT2D, deixen d’activar-se els receptors d’estrògens. Experiments realitzats amb ratolins han mostrat que eliminar la KMT2D i alhora inhibir la PI3K aconsegueix reduir els tumors de manera eficaç.
Aquests resultats suggereixen dues possibles estratègies per combatre els càncers de mama metastàtics amb mutacions al gen que produeix la proteïna PI3K.
Una opció és combinar dos fàrmacs, un per inhibir PI3K i l’altre per inhibir els receptors d’estrògens. D’aquesta manera, es continuaria activant la proteïna KMT2D però deixaria de tenir un efecte perjudicial, perquè no trobaria receptors d’estrògens sobre els quals actuar.
Ja hi ha dos assajos clínics en curs, tots dos amb participació d’hospitals espanyols, per provar aquesta estratègia. Els resultats se sabran aquest mateix any. “Si són positius, es convertirà en el nou estàndard per al tractament de tumors de mama amb receptors hormonals positius i mutacions del gen PIK3CA”, que produeix la proteïna PI3K, vaticina Baselga.
La segona opció, que trigarà més a donar fruits, consisteix a atacar directament la proteïna KMT2D. Ara mateix “no hi ha cap inhibidor específic d’aquesta proteïna, però és una diana terapèutica prometedora”, afegeix el director mèdic de l’hospital Memorial Sloan Kettering. “Ja estem treballant per produir fàrmacs contra la KMT2D. És un dels nostres nous projectes”.
Hi ha altres tipus de càncer en els quals s’ha observat la influència de factors epigenètics. Entre ells, els de pròstata, algunes leucèmies i limfomes. Ja s’han desenvolupat fàrmacs per contrarestar alteracions epigenètiques en aquests càncers. La nova investigació és la primera que identifica mecanismes epigenètics en la progressió del càncer de mama.
Segons Baselga, “aquesta investigació és un exemple perfecte de com les observacions clíniques poden guiar la recerca fonamental. La reactivació dels receptors d’estrògens explica la resistència a molts tractaments i les recidives tardanes en molts casos de càncer de mama. El mecanisme epigenètic que hem descobert és una peça més del puzle, possiblement una de les més centrals. Estem estrenyent el setge. El meu somni és poder evitar que la cèl·lula tumoral tingui capacitat de reacció immediata. La manera d’aconseguir-ho és atacant mecanismes epigenètics”.